
30批次医疗器械抽检不合格 甘肃人快看你家有吗


独家抢先看
甘肃省药品监督管理局关于发布2024年医疗器械
监督抽检结果的通告
(2025年第2号)
为加强医疗器械监督管理,保障医疗器械产品质量安全有效,甘肃省药监局组织对全省医疗器械生产、经营和使用单位中一次性使用无菌注射器(带针)、玻璃体温计、一次性口腔器械盒、脉搏血氧仪等40个品种进行产品质量监督抽检,发现30批产品不符合标准规定。具体情况如下:
一、被抽检项目不符合标准规定的产品
(一)玻璃体温计28批次,分别为江苏华辰医用仪表有限公司(2批次)、宁波鄞州华鑫仪器有限公司(1批次)、江苏辰宇医疗器械有限公司(5批次)、陕西省医疗仪器厂(5批次)、扬州华祥医疗器械有限公司(4批次)、洪江市正兴医疗仪表厂(1批次)、宁波市海曙华合玻璃仪表有限公司(4批次)、重庆日月医疗设备有限公司(2批次)、万年县芯智微科技有限公司(2批次)、安徽方达药械股份有限公司(1批次)、南昌市江南诚医疗器械有限公司(1批次)生产,涉及示值、难甩等项目不符合标准规定。
(二)脉搏血氧仪1批次,河南友倍康医疗器械有限公司生产,涉及脉率项目不符合标准规定。
(三)一次性使用口腔器械盒1批次,石家庄市圣彤医药用品厂生产,涉及无菌项目不符合标准规定。
以上抽检不符合标准规定产品具体情况见附件。
二、监管要求
对抽检中发现的上述不符合标准规定的产品,甘肃省药监局已要求被抽查单位所在市州市场监管局按照《医疗器械监督管理条例》《医疗器械生产监督管理办法》《医疗器械召回管理办法》等要求,及时作出行政处理决定并向社会公布。市州市场监管局要督促辖区内经营使用单位对抽检不符合标准规定的同批次产品全面排查并进行风险评估,根据医疗器械缺陷严重程度确定召回级别,主动召回产品并公开召回信息,制定整改措施并按期整改到位。
特此通告。
附件:抽检不符合标准规定产品名单
甘肃省药品监督管理局
2025年1月21日
附件

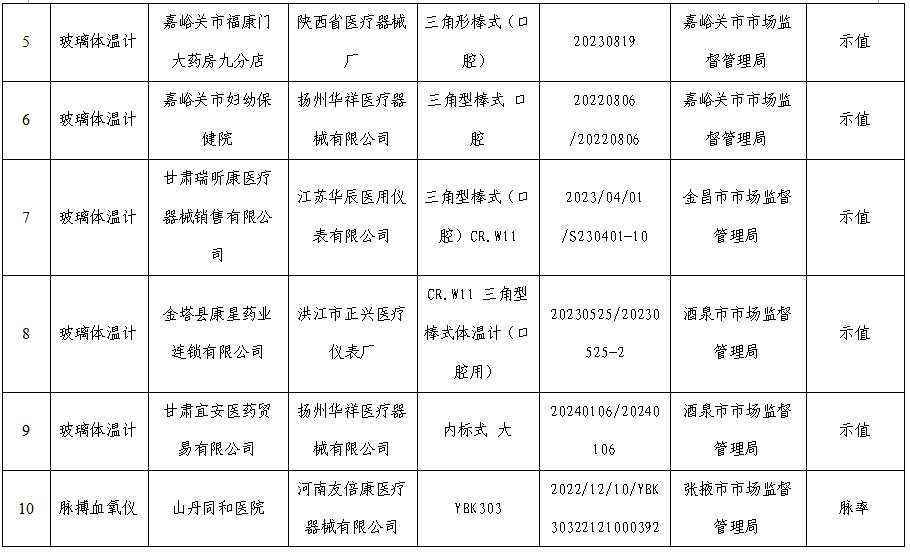



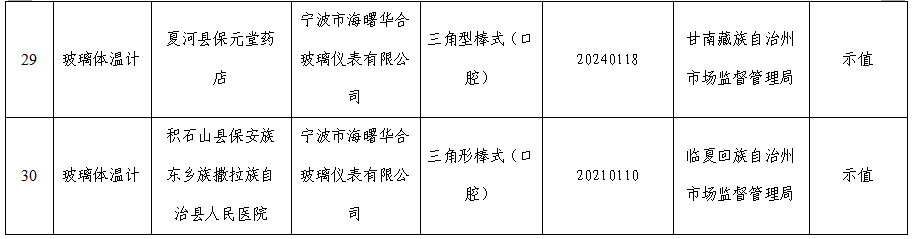
(甘肃省药品监督管理局官方公众号)






