
张元豪等团队Cell:重构癌症基因组认知


独家抢先看
原标题:张元豪等团队Cell:重构癌症基因组认知

生命科学
Life science
染色体外DNA(ecDNA)扩增是人类癌症的关键驱动因素。2026年1月7日,斯坦福大学张元豪(Howard Y.Chang)团队在Cell Press细胞出版社旗下期刊Cell上在线发表题为“EcDNA-borne structural variants drive oncogenic fusion transcript amplification”的研究论文,该研究表明ecDNA是在不同癌症类型中产生和扩增癌基因融合转录物的主要平台。
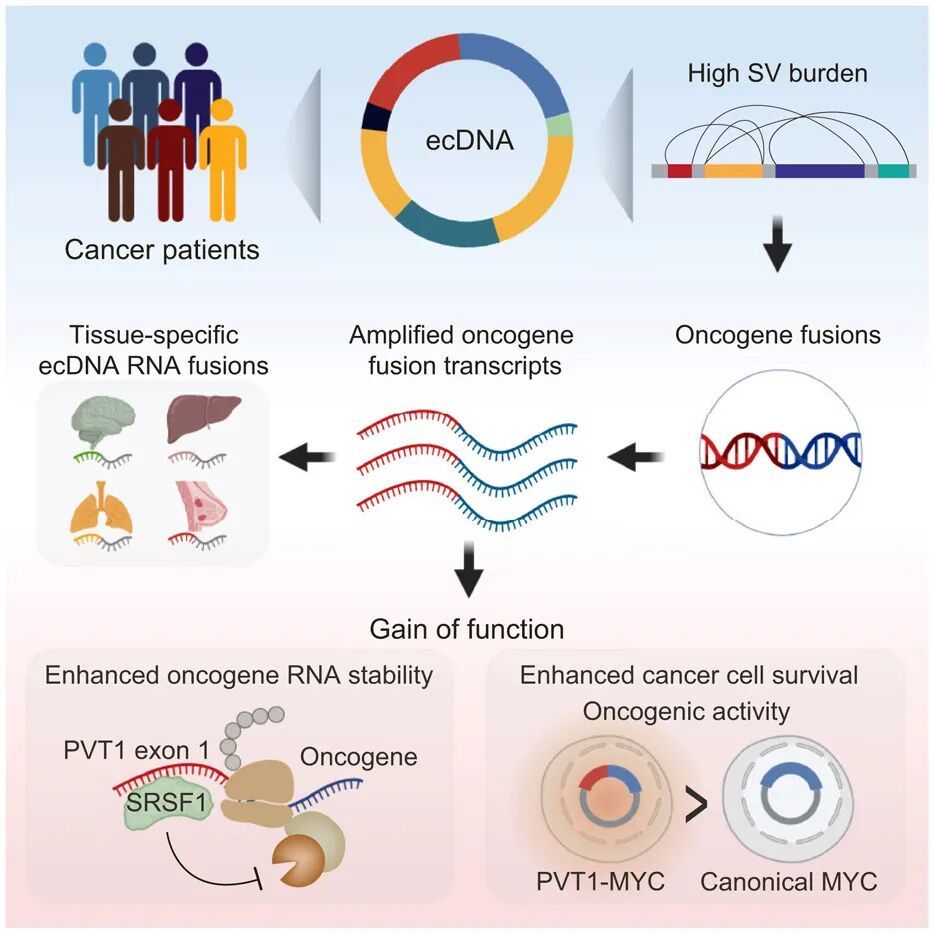
通过对肿瘤样本和各种组织类型的癌细胞系的全基因组和转录组序列的综合分析,该研究发现在任何拷贝数改变中,ecDNAs具有最高的癌基因融合事件发生率。关注最常见的ecDNA融合热点,该研究发现长链非编码RNA基因PVT1的5’端与外显子1连接到不同的3’伴侣的融合,可能通过SRSF1依赖的机制提高了RNA的稳定性,并增强了MYC依赖的转录和癌细胞的存活。这些结果表明,在癌症中,ecDNA促进了基因组的不稳定性和频繁的癌基因融合形成。
染色体外DNA(ecDNA)是兆碱基对大小的环状片段,编码癌基因和其他有利于肿瘤适应性的遗传元件,驱动癌基因扩增、肿瘤内遗传异质性、肿瘤快速进化和治疗耐药性。在成人癌症类型中,17.1%的肿瘤中检测到ecDNA衍生扩增,在转移性肿瘤中频率增加,并且与较短的生存期相关。
ecDNA代表了基因组不稳定的主要形式,通过非孟德尔遗传驱动基因组重排和快速选择以获得适合变异,导致患者预后不良。晚期和转移性肿瘤表现出ecDNA拷贝数和结构复杂性的增加,在ecDNA扩增的癌基因位点中,结构变异(SV)负担尤其升高,强调了ecDNA驱动的基因组不稳定性在侵袭性癌症进展中的作用。
基因组重排——包括易位、倒位、插入和缺失——当不同基因的片段异常地连接在一起时,可以产生基因融合。基因融合是许多癌症的标志,但在正常组织中很少见。高SV负荷促进基因融合,导致启动子劫持或融合转录物形成,破坏基因调控,驱动肿瘤发生。有趣的是,多项研究表明,基因融合和不同癌症类型的基因组扩增之间存在很强的关联。最近的证据表明,ecDNA和基因融合之间存在潜在的联系,因为在ecDNA上发现了反复截断的基因。然而,ecDNA在驱动产生基因融合的SVs中的作用及其功能后果仍不清楚。
该研究系统地检测了与ecDNA相关的基因融合,证明了ecDNA驱动的基因组不稳定性是人类癌症中致癌基因融合的主要来源。该研究进一步关注最常见的ecDNA融合热点,浆细胞瘤变异易位1(PVT1),揭示ecDNA依赖性融合促进癌症致癌调节的潜在机制。

相关论文信息
相关论文刊载于CellPress细胞出版社
▌论文标题:
EcDNA-borne structural variants drive oncogenic fusion transcript amplification
▌论文网址:
https://www.sciencedirect.com/science/article/pii/S0092867425014229
▌DOI:
https://doi.org/10.1016/j.cell.2025.12.009
原标题:《张元豪等团队Cell:重构癌症基因组认知:ecDNA驱动癌基因融合转录本产生,成为肿瘤进化的核心引擎|Cell Press论文速递》






